- Top
- アキャルックス®製品ページ
- 臨床成績について(国内データ)
臨床成績について
国内第Ⅰ相試験(RM-1929-102試験)1)
1)社内資料:RM-1929-102試験(2020年9月25日承認、CTD 2.7.6.2)_承認時評価資料
警告を含む使用上の注意等の詳細は
アイコン製品基本情報(添付文書等)をご参照ください。
試験概要
試験デザイン
単一施設、非盲検試験
目的
切除不能な局所再発の日本人頭頸部扁平上皮癌患者におけるアキャルックス®を用いた本治療の安全性、薬物動態、予備的な有効性、免疫原性の検討
対象
切除不能な局所再発の日本人頭頸部扁平上皮癌患者:3例
(アキャルックス®を投与した全患者を有効性解析対象(ITT集団)及び安全性解析対象とした)
方法
アキャルックス®640mg/㎡を2時間以上かけて点滴静注し(Day 1)、投与終了約24時間後に(Day 2)レーザシステムを用いて治療の標的とする病変にレーザ光照射(表在性病変:50J/cm2、深在性病変:100J/cm)する治療を1サイクル実施した。
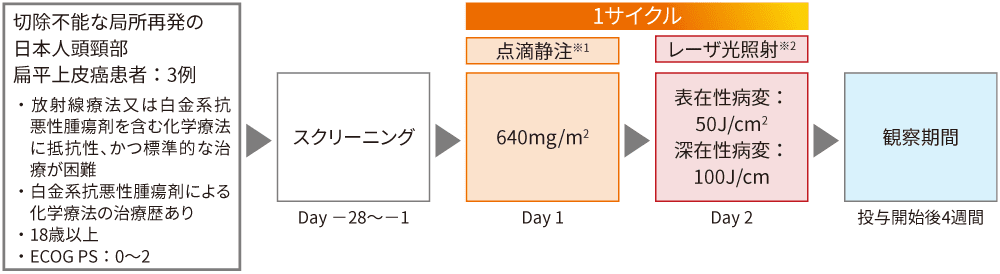
- ※1:セツキシマブ100mgのチャレンジ投与を行い忍容性が良好であった患者を対象に2時間以上かけて点滴静注した
- ※2:アキャルックス®投与終了20~28時間後
主要評価項目
安全性
副次評価項目
薬物動態プロファイル、奏効率及び病勢コントロール率に基づく抗腫瘍効果(modified RECIST ver.1.1※3、Choi基準及びPERCISTに基づき評価)、免疫原性反応(抗薬物抗体[ADA])等
解析計画
主要な抗腫瘍効果はmodified RECIST ver.1.1に基づいて評価した。
患者背景
| 安全性解析対象集団:3例 | ||
|---|---|---|
| 年齢 歳 | 平均値(SD) | 65.0(10.82) |
| 範囲 | 50-70代 | |
| 年齢層 | 65歳未満 | 1(33.3%) |
| 65歳以上 | 2(66.7%) | |
| 性別 | 男性 | 0 |
| 女性 | 3(100%) | |
| 体表面積 ㎡ | 平均値(SD) | 1.437(0.1115) |
| 中央値(範囲) | 1.480(1.31-1.52) | |
| ECOG PS | 0 | 2(66.7%) |
| 1 | 1(33.3%) | |
| 2 | 0 | |
| 原発部位 | 歯肉 | 1(33.3%) |
| 中咽頭 | 1(33.3%) | |
| その他(外耳) | 1(33.3%) | |
抗腫瘍効果[副次評価項目]
3例中2例に部分奏効(PR)、1例に病勢進行(PD)が認められた。奏効及び病勢コントロールはともに3例中2例に認められた。
抗腫瘍効果
| ITT集団:3例 | ||
|---|---|---|
| 最良総合効果 | CR | 0例 |
| PR | 2例 | |
| SD | 0例 | |
| PD | 1例 | |
| 完全奏効率(CR) | 0/3例 | |
| 奏効率(CR+PR) | 2/3例 | |
| 病勢コントロール率(CR+PR+SD) | 2/3例 | |
modified RECIST ver.1.1に基づく中央判定による評価
modified RECIST ver.1.1における病変の評価方法はRECIST ver.1.1に準拠しており、本治療は局所治療であることから、標的病変の選択方法にのみ変更が適用された。RECIST ver.1.1からの変更点は以下のとおりである。
【modified RECIST ver.1.1】
- 本治療で治療した病変を標的病変、本治療で治療しなかった病変を非標的病変とする。
- 本治療で治療した病変はすべて標的病変として選択することとし、RECIST ver.1.1の標的病変の基準(標的病変として選択する病変数は1臓器あたり最大2病変かつ合計最大5病変、標的病変の大きさはリンパ節以外の病変で長径10mm以上、リンパ節の短径で15mm以上)は適用しない。
- 各評価時点の腫瘍縮小効果は、標的病変(本治療で治療した病変)、非標的病変(本治療で治療しなかった病変)及び新病変の有無の評価に基づき総合的に判定する。
- 標的病変の腫瘍縮小効果は本治療で治療した病変の腫瘍縮小効果とする。
安全性[主要評価項目]
有害事象は全3例(100%)に17件認められ、このうち13件は治験治療との関連があると判断された。重篤な有害事象、死亡及び治療中止に至った有害事象は認められなかった。DLT(Dose-Limiting Toxicity)観察期間中(Day 1~Day 7)にDLTの発現は認められなかった。
治験薬投与後に発現した有害事象
| 安全性解析対象集団:3例 | |
|---|---|
| 治験薬投与後に発現した有害事象 | 3(100.0%) |
| 一般・全身障害および投与部位の状態 | 3(100.0%) |
| 適用部位疼痛 | 3(100.0%) |
| 適用部位浮腫 | 1(33.3%) |
| 顔面浮腫 | 1(33.3%) |
| 限局性浮腫 | 1(33.3%) |
| 臨床検査 | 2(66.7%) |
| 血圧上昇 | 1(33.3%) |
| γ-グルタミルトランスフェラーゼ増加 | 1(33.3%) |
| 白血球数減少 | 1(33.3%) |
| 血液およびリンパ系障害 | 1(33.3%) |
| 貧血 | 1(33.3%) |
| 胃腸障害 | 1(33.3%) |
| 舌炎 | 1(33.3%) |
| 肝胆道系障害 | 1(33.3%) |
| 肝機能異常 | 1(33.3%) |
| 皮膚および皮下組織障害 | 1(33.3%) |
| 全身性皮疹 | 1(33.3%) |
MedDRA ver.21.0